ТЕМА НОМЕРА: ПРЕПАРАТЫ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ И ИММУНОГЛОБУЛИНОВ: ОТ РАЗРАБОТКИ ДО КЛИНИЧЕСКОГО ПРИМЕНЕНИЯ
ВВЕДЕНИЕ. Бешенство является абсолютно смертельным заболеванием при отсутствии адекватной антирабической помощи, которая в ряде случаев требует введения препаратов антирабического иммуноглобулина (АИГ) в сочетании с антирабической вакциной. Учитывая проблемы с поставками АИГ, получаемого из донорской крови, в мире ведутся разработки препаратов на основе нейтрализующих антирабических моноклональных антител (МкАТ), которые могут быть востребованы и в российской системе здравоохранения.
ЦЕЛЬ. Описательный обзор результатов разработки, клинических и пострегистрационных исследований безопасности и эффективности препаратов антирабических моноклональных антител, предназначенных для постэкспозиционной профилактики бешенства в комбинации с антирабической вакциной.
ОБСУЖДЕНИЕ. В настоящее время в мире зарегистрированы три препарата антирабических МкАТ: два препарата в Индии — рекомбинантное человеческое антирабическое антитело и комбинированный препарат докаравимаба и миромавимаба; один препарат в Китае — ормутивимаб. Доклинические исследования подтвердили способность препаратов нейтрализовать вирус бешенства, в том числе уличные штаммы. В ходе проведения клинических исследований был установлен благоприятный профиль безопасности препаратов антирабических МкАТ (большинство нежелательных явлений носили транзиторный характер и разрешались самостоятельно) и отсутствие иммунной интерференции с вводимыми антирабическими вакцинами. Применение всех перечисленных препаратов не приводило к изменению иммунного ответа на завершенный курс вакцинации антирабической вакциной по сравнению с препаратами человеческого АИГ — на 42 сут исследования (через 4 нед. после введения последней дозы антирабической вакцины) титры вируснейтрализующих антител достигали 31,12 МЕ/мл для препарата рекомбинантного человеческого антирабического антитела и 122 МЕ/мл для комбинированного препарата докаравимаба и миромавимаба. В ходе контролируемых клинических исследований и пострегистрационных исследований препарата рекомбинантного человеческого антирабического антитела и комбинированного препарата докаравимаба и миромавимаба не было зарегистрировано эпизодов заболевания бешенством у пациентов, получавших постэкспозиционную профилактику исследуемыми препаратами и антирабической вакциной.
ЗАКЛЮЧЕНИЕ. Препараты антирабических МкАТ представляют собой эффективную и безопасную альтернативу при реализации схемы постэкспозиционной профилактики бешенства, что подтверждено мировым опытом их применения. Внедрение таких препаратов в практику комплексной антирабической помощи в Российской Федерации позволит преодолеть потенциальный дефицит препаратов антирабических иммуноглобулинов. Ключевыми задачами для регистрации препаратов антирабических МкАТ являются оценка их кросс-реактивности с тканями человека ex vivo и подтверждение нейтрализующей активности против вирусных изолятов, циркулирующих в России и сопредельных государствах.
ВВЕДЕНИЕ. Перспективным направлением постэкспозиционной профилактики бешенства является применение препаратов на основе моноклональных антител (МкАТ). В связи с отсутствием на фармацевтическом рынке российских препаратов МкАТ для профилактики бешенства целесообразно проведение доклинической оценки защитной эффективности комбинированного препарата на основе докаравимаба и миромавимаба против циркулирующих на территории Российской Федерации уличных штаммов вируса бешенства.
ЦЕЛЬ. Исследование защитной эффективности комбинированного препарата антирабических моноклональных антител докаравимаба и миромавимаба в отношении актуальных для Российской Федерации штаммов классического вируса бешенства в эксперименте на мышах BALB/с.
МАТЕРИАЛЫ И МЕТОДЫ. В качестве тестируемого препарата использовали комбинированный препарат антирабических МкАТ докаравимаба и миромавимаба, в качестве препарата сравнения — иммуноглобулин антирабический Ребинолин. Применяли уличные штаммы вируса бешенства: 777-М, Россия/Самара/2018, RABV/Russia/SP48SolMak/2020; фиксированный штамм CVS. При изучении эффективности использовали 960 мышей линии BALB/с (480 самок, 480 самцов), сформировав 23 группы по 20 животных в каждой (10 самцов, 10 самок). Мышей групп № 3–18 внутримышечно инфицировали вирусом бешенства, а через 6 или 24 ч внутримышечно вводили комбинированный препарат или препарат сравнения. Мышам групп № 1 и 2 вводили 0,9% раствор натрия хлорида (плацебо). Мыши групп № 19–22 служили контролем дозы вируса, а группы № 23 — интактным контролем. Для оценки защитной эффективности препарата проводили взвешивание мышей, определяли инкубационный и клинический периоды, показатели средней продолжительности жизни мышей до гибели, показатели защиты животных от проявления клинических признаков и от гибели. Оценку инфекционной активности вируса проводили на мышах BALB/с при интрацеребральном инфицировании. Специфичность гибели животных подтверждали с помощью ОТ-ПЦР-РВ.
РЕЗУЛЬТАТЫ. Введение мышам комбинированного препарата на основе докаравимаба и миромавимаба приводило к достоверному увеличению массы тела, средней продолжительности жизни и защите от клинических проявлений бешенства у инфицированных мышей по сравнению с группами контроля дозы вируса. Комбинированный препарат демонстрировал высокую защитную эффективность в отношении штаммов вируса бешенства и не уступал по эффективности препарату сравнения. Введение комбинированного препарата через 6 ч после инфицирования (штаммы 777-М, Россия/Самара/2018, RABV/Russia/SP48SolMak/2020, CVS) обеспечивало защиту от гибели 90–100% самцов и самок мышей, а через 24 ч — 90–100% самцов и 96–100% самок мышей.
ВЫВОДЫ. В эксперименте на мышах установлена высокая защитная эффективность комбинированного препарата на основе докаравимаба и миромавимаба против актуальных для Российской Федерации уличных штаммов классического вируса бешенства. Комбинированный препарат не уступал по защитной эффективности препарату сравнения, что позволяет его рекомендовать для дальнейших доклинических и клинических исследований.
ВВЕДЕНИЕ. Оценка фармакокинетики препаратов на основе моноклональных антител требует тщательного выбора релевантных моделей животных для обеспечения трансляционной значимости данных. Для решения этой проблемы проведена оценка фармакокинетических параметров двух человеческих моноклональных антител, нейтрализующих SARS-CoV-2, на двух видах лабораторных животных — сирийских хомяках и мышах.
ЦЕЛЬ. Оценка фармакокинетических параметров моноклональных антител человека IgG1 каппа (МКАТ iC1 и МКАТ iB20), нейтрализующих SARS-CoV-2, после однократного внутривенного введения сирийским хомякам и аутбредным мышам линии ICR CD1.
МАТЕРИАЛЫ И МЕТОДЫ. Пилотное исследование выполнено на 15 самцах сирийских хомяков, которым однократно внутривенно вводили МКАТ iC1 в дозе 5 мг/кг. Отбор проб крови проводили до введения и в 10 временных точках в течение 144 ч. В основном исследовании мышам ICR CD1 (4 группы по 60 животных) однократно внутривенно вводили МКАТ iC1 и МКАТ iB20 в дозах 5 и 50 мг/кг. Отбор проб крови проводили до введения и в 11 временных точках в течение 504 ч. Концентрацию антител в сыворотке крови определяли методом иммуноферментного анализа (ИФА). Методики ИФА валидировали по следующим показателям: селективность, нижний предел количественного определения, калибровочный диапазон, правильность, прецизионность, стабильность аналита. Фармакокинетические параметры (максимальная концентрация — Cmax, площадь под кривой «концентрация — время» — AUC0–t, среднее время удерживания — MRT, период полувыведения — T1/2, клиренс — Cl) рассчитывали внемодельным методом статистических моментов.
РЕЗУЛЬТАТЫ. Валидированы методики иммуноферментного определения МКАТ iC1 и iB20 в сыворотке крови мышей в аналитическом диапазоне 1,25–25,0 и 1,5–20,0 мкг/мл соответственно. Параметры Cmax, AUC0–t, AUC0–∞ статистически значимо возрастали с увеличением дозы для обоих антител. После введения мышам МКАТ iC1 в дозах 5 и 50 мг/кг значения Cmax составили около 235 и 1228 мкг/мл, AUC0–t — 6458 и 71 193 ч×мкг/мл. Для МКАТ iB20 значения Cmax составили около 359 и 4442 мкг/кг, AUC0–t — 6344 и 76 251 ч×мкг/мл соответственно. Параметры MRT и T1/2 не зависели от введенной дозы. В совокупности с низкими значениями клиренса это свидетельствует о длительной циркуляции аналитов в системном кровотоке.
ВЫВОДЫ. Определены фармакокинетические параметры МКАТ iC1 и iB20 при однократном введении сирийским хомякам и мышам ICR CD1. Установлена дозозависимость ключевых параметров (Cmax, AUC0–t). Полученные результаты служат основанием для дальнейшей доклинической и клинической разработки препаратов.
ВВЕДЕНИЕ. Несмотря на значительное снижение заболеваемости острым гепатитом В (ГВ) благодаря вакцинопрофилактике, экстренная специфическая профилактика ГВ остается актуальной проблемой для глобального здравоохранения и здравоохранения Российской Федерации. Совершенствование методов экстренной профилактики, в частности переход на внутривенные формы специфического иммуноглобулина, обладающие более высокой биодоступностью и способностью быстро создавать защитный титр антител, позволит обеспечить надежную защиту лицам в группах высокого риска заражения ГВ. В Российской Федерации иммуноглобулины человека (ИГЧ) против ГВ представлены препаратом Антигеп (Россия) для внутримышечного введения и зарубежным препаратом Неогепатект (Германия) для внутривенного введения. Для совершенствования иммунопрофилактики ГВ и реализации политики импортозамещения актуальны исследования по разработке первого российского лекарственного препарата ИГЧ против ГВ для внутривенного введения.
ЦЕЛЬ. Разработка, контроль качества, исследование вирусной безопасности и фармакокинетики российского препарата иммуноглобулина человека против гепатита В для внутривенного введения.
МАТЕРИАЛЫ И МЕТОДЫ. ИГЧ против ГВ (Антигеп-Нео) получали из плазмы крови доноров с высоким уровнем антител к вирусу ГВ. Качество препарата оценивали по физико-химическим, биологическим и молекулярным параметрам, содержанию иммуноглобулина А, функциональному состоянию Fc-фрагмента и тромбогенному потенциалу. Фармакокинетику изучали в рамках доклинических (кролики) и клинических (добровольцы) исследований. Препараты Неогепатект и Антигеп использовали в качестве препаратов сравнения.
РЕЗУЛЬТАТЫ. Технология получения ИГЧ основана на стандартном спиртовом фракционировании по методу Кона с последующей хроматографической очисткой и трех стадиях удаления и инактивации вирусов. Полученный препарат демонстрировал вирусную безопасность и содержит более 95% действующего вещества — иммуноглобулины класса G (IgG), из которых более 99% — мономеры и димеры. Препарат характеризовался низкой антикомплементарной активностью (0,17±0,06 СН50/мг IgG), низким содержанием активатора прекалликреина (7,45±2,11 МЕ/мл) и отсутствием тромбогенного потенциала. Биоэквивалентность препаратов Антигеп-Нео и Неогепатект подтверждена в доклинических и клинических исследованиях. Фармакокинетические параметры сравниваемых препаратов статистически не различались.
ВЫВОДЫ. Разработанный иммуноглобулин человека против гепатита В (препарат Антигеп-Нео) соответствует нормативным требованиям по качеству и вирусной безопасности. Доклинические и клинические исследования подтвердили близкую фармакокинетику Антигеп-Нео и препарата сравнения Неогепатект.
ВВЕДЕНИЕ. Применение стандартных образцов (СО) — неотъемлемая часть метрологического обеспечения аналитических методик в фармацевтическом производстве. Системный анализ литературы в области стандартизации лекарственных препаратов иммуноглобулинов человека (ИГЧ), в частности специфических и специального назначения, позволит оценить уровень метрологического обеспечения в Российской Федерации, определить новые подходы к получению и применению СО для оценки специфической активности.
ЦЕЛЬ. Провести анализ данных литературы о спектре стандартных образцов, используемых для оценки специфической активности лекарственных препаратов иммуноглобулинов человека в Российской Федерации и за рубежом.
ОБСУЖДЕНИЕ. Информационный поиск в PubMed, eLIBRARY.RU и справочно-правовой системе КонсультантПлюс® показал, что номенклатура Международных стандартных образцов (МСО) для оценки специфической активности ИГЧ представлена МСО ИГЧ антирезус Rh0(D), ИГЧ против гепатита В, противостолбнячного, противостафилококкового, антицитомегаловирусного, антирабического и противооспенного. МСО ИГЧ против клещевого энцефалита отсутствует, поскольку в странах Европейского союза специфический ИГЧ не выпускается. При этом отмечается полная зависимость от импорта МСО для оценки специфической активности ИГЧ антицитомегаловирусного, ИГЧ против гепатита B и ИГЧ антирабического. Как правило, МСО производят на основе готовых серий соответствующих лекарственных препаратов, стабилизируют, разливают в стерильных условиях и лиофилизируют. В свою очередь, реестр СО Государственной фармакопеи Российской Федерации включает фармакопейные стандартные образцы (ФСО) ИГЧ антирезус Rh0(D), противостолбнячной сыворотки и содержания антиальфастафилолизина. В отличие от МСО, ФСО выпускаются в форме растворов, что снижает стабильность антител. Для ФСО устанавливают статистическую неопределенность аттестованного значения, однако при аттестации МСО установление такой характеристики не является обязательной. Кроме того, анализ литературных данных позволил выявить, что стабильность и близость по составу и свойствам к стандартизуемым лекарственным средствам представляют собой ключевые требования к СО. Российские и зарубежные требования к аттестации СО различаются. Число российских СО на основе ИГЧ класса G ограничено, поскольку СО чаще всего получают из сыворотки крови лошади. Сведения о СО ИГЧ противооспенного не обнаружены.
ЗАКЛЮЧЕНИЕ. Российская фармацевтическая промышленность недостаточно обеспечена национальными СО для оценки специфической активности лекарственных препаратов ИГЧ и донорской плазмы для их производства, поэтому необходимы выпуск таких СО в форме лиофилизата и аттестация в международных единицах с оценкой статистической неопределенности значения содержания антител.
ДОКЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ БИОЛОГИЧЕСКИХ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ
ВВЕДЕНИЕ. Одна из причин роста заболеваемости коклюшем заключается в адаптации патогена к имеющемуся коллективному иммунитету, сформированному в условиях вакцинопрофилактики заболевания. Мониторинг иммунобиологических свойств штаммов Bordetella pertussis необходим для прослеживания изменений адаптивного потенциала патогена в ответ на вакцинацию.
ЦЕЛЬ. Сопоставление иммунобиологических свойств выделенных изолятов циркулирующих штаммов Bordetella pertussis и производственных штаммов, используемых для изготовления цельноклеточной коклюшной вакцины.
МАТЕРИАЛЫ И МЕТОДЫ. В исследовании использованы 9 изолятов современных циркулирующих штаммов B. pertussis, выделенных от пациентов с коклюшем в 2016–2020 гг. Из штаммов изготовлены экспериментальные серии цельноклеточной коклюшной вакцины. Серии оценивали по следующим параметрам: серологические свойства и антигенная структура (серотипы); гемагглютинирующая, гемолитическая и дермонекротическая активности; вирулентность; остаточная токсичность и защитная активность. В исследовании использовали аутбредных и инбредных мышей линии F1 (C57Bl/6J×CBA). Бактериальную культуру оценивали по морфологическим и культуральным свойствам. Экспериментальные данные сопоставляли с требованиями к производственным штаммам, изложенным в МУК 4.2.2317-08 (Отбор, проверка и хранение производственных штаммов коклюшных, паракоклюшных и бронхисептикозных бактерий).
РЕЗУЛЬТАТЫ. Из 9 изолятов циркулирующих штаммов B. pertussis выделены штаммы 16-16 и 33-18, которые соответствуют требованиям к производственным штаммам. Анализ результатов оценки защитной активности штаммов 25-16, 37-18 и 2-20 указал на целесообразность дополнительного подтверждения данного показателя из-за ограниченности опытного материала. Четыре штамма 31(2)-17, 28(1)-18, 25-16, 2-20 B. pertussis не проявили требуемой защитной активности (<8 МЕ/мл).
ВЫВОДЫ. Свойства изолятов 16-16 и 33-18 B. pertussis соответствуют всем требованиям к производственным штаммам. Исследованные штаммы имеют современный генотип и перспективны с точки зрения их практического использования в качестве кандидатов для замены устаревших производственных штаммов B. pertussis при изготовлении коклюшных вакцин.
ВВЕДЕНИЕ. Препараты на основе бактериальных антигенов эффективны для профилактики инфекций, вызываемых условно-патогенными бактериями, однако их промышленное использование требует оптимизации состава и технологии получения антигенов. Перспективным подходом является разработка комплекса антигенов Klebsiella pneumoniae, Escherichia coli, Proteus vulgaris и Staphylococcus aureus.
ЦЕЛЬ. Изучение защитных свойств и токсичности антигенов K. pneumoniae, E. coli, P. vulgaris и S. aureus, а также комплекса антигенов в эксперименте на мышах.
МАТЕРИАЛЫ И МЕТОДЫ. В работе использовали антигены K. pneumoniae 204, E. coli F147, P. vulgaris 177 и суммарный антиген двух штаммов S. aureus (1986 и 1991), а также комплекс, состоящий из перечисленных антигенов. Токсичность оценивали на белых мышах линии SHK обоего пола массой 18–20 г. Животным однократно внутрибрюшинно вводили антигены (50, 100 или 200 мкг на мышь) или комплекс антигенов (0,1; 0,2; 0,4; 0,6 мл на мышь). Защитные свойства комплекса антигенов (в дозе 0,1 мл) изучали на самках мышей линии SHK массой 14–16 г. После двукратной иммунизации животных заражали живыми культурами гомологичных штаммов (K. pneumoniae 204, E. coli F147, P. vulgaris 177, S. aureus 1986) и гетерологичным штаммом P. aeruginosa PA103. В течение 7 сут регистрировали выживаемость и рассчитывали значение ЛД50 и индекса эффективности.
РЕЗУЛЬТАТЫ. Установлено, что антигены E. сoli, S. aureus и P. vulgaris (во всех дозах) и антигены K. pneumoniae (в дозах 50 и 100 мкг) не вызывали токсические эффекты у мышей. Введение мышам антигена K. pneumoniae в дозе 200 мкг приводило к снижению массы тела и гибели животных. Инъекция комплекса антигенов в диапазоне доз 0,1–0,4 мл не вызывала токсических эффектов, а при введении дозы 0,6 мл выявлены признаки токсичности. Двукратная иммунизация комплексом антигенов в дозе 0,1 мл обеспечивала защиту мышей от заражения гомологичными и гетерологичными штаммами. Значения индекса эффективности составили: 7,99 для K. pneumoniae 204; 11,56 для E. coli F147; 25,90 для P. vulgaris 177; 7,45 для S. aureus 1986; 4,00 для P. aeruginosa PA103 (р<0,05).
ВЫВОДЫ. Исследованные антигены K. pneumoniae, E. coli, P. vulgaris и S. aureus, а также комплекс антигенов обладали приемлемым токсикологическим профилем. Комплекс антигенов продемонстрировал выраженные защитные свойства как против гомологичных штаммов (K. pneumoniae, E. coli, P. vulgaris, S. aureus), так и против гетерологичного штамма P. aeruginosa. Исследованные антигены и их комплекс могут рассматриваться как основа для создания лекарственного средства для профилактики широкого круга инфекций, вызванных условно-патогенными бактериями.
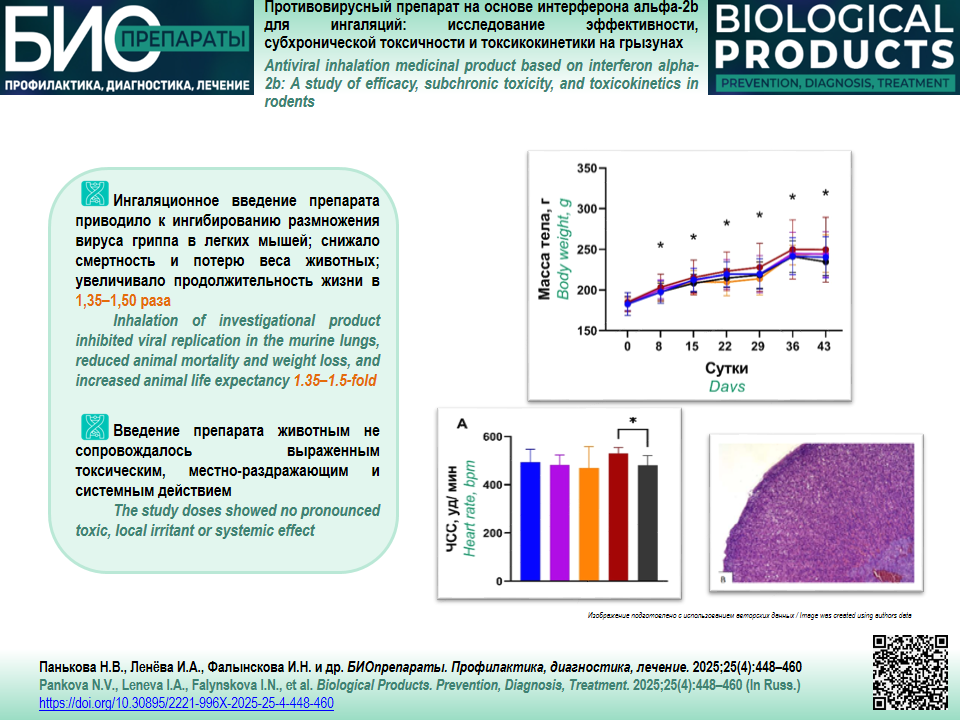
ВВЕДЕНИЕ. Актуальность разработки новых высокодозных интерферон-содержащих лекарственных препаратов (ЛП) в виде капель для ингаляций обусловлена необходимостью создания эффективных средств для этиотропной терапии острых респираторных вирусных инфекций (ОРВИ), гриппа и COVID-19, сочетающих прямое действие на слизистую оболочку, мощный иммунный ответ и благоприятный профиль безопасности. В 2021 г. был разработан новый ЛП на основе интерферона альфа-2b в виде капель для ингаляций, предназначенный для лечения гриппа и ОРВИ различной этиологии.
ЦЕЛЬ. Доклиническое исследование эффективности, субхронической токсичности и токсикокинетики нового лекарственного препарата на основе интерферона альфа-2b при ингаляционном пути введения.
МАТЕРИАЛЫ И МЕТОДЫ. ЛП создан на основе человеческого рекомбинантного интерферона альфа-2b. Исследование эффективности ЛП было проведено на самках мышей BALB/c. Животным проводили ингаляцию 3 мл исследуемого ЛП в течение 10 мин ежедневно 2 раза/сут в течение 8 сут. Заражение вирусом гриппа А/Калифорния/04/2009 (A(H1N1)pdm2009) проводили на 2 сут ингаляций. Оценивали динамику массы тела и смертности животных, а также титр вируса гриппа в тканях легких мышей через 4 сут после заражения. Токсичность ЛП исследовали на белых нелинейных крысах обоих полов. ЛП вводили с помощью ингалятора 1 раз/сут в течение 7 нед. в дозах, превышающих в 5,3 и 53 раза терапевтическую дозу для человека. Патоморфологическое и патогистологическое исследования проводили на 29 и 43 сут от начала введения ЛП. Исследования гематологических и биохимических показателей крови, частоты сердечных сокращений и поведенческих функций проводили до введения ЛП, во время введения (4-я нед.) и после окончания введения ЛП через 2 нед. Изучение токсикокинетики проводили на сателлитных группах самцов крыс; схема введения ЛП животным была аналогичной схеме исследования токсичности.
РЕЗУЛЬТАТЫ. В экспериментах установлено, что ингаляционное введение (923 000 МЕ/кг/сут, 2 раза/сут в течение 8 сут) исследуемого ЛП приводило к ингибированию размножения вируса гриппа А/Калифорния/04/2009 (A(H1N1)pdm2009) в легких мышей, достоверно снижало смертность и потерю веса животных, увеличивало продолжительность жизни в 1,35–1,50 раза. Введение ЛП животным в изученных дозах не сопровождалось выраженным токсическим, местно-раздражающим и системным действием.
ВЫВОДЫ. В доклинических исследованиях доказана эффективность и безопасность исследуемого ЛП при ингаляционном введении грызунам.
ПРОТИВОВИРУСНЫЕ ВАКЦИНЫ
ВВЕДЕНИЕ. Вирус ветряной оспы (ВВО) остается серьезной угрозой для здоровья населения и представляет собой значительное бремя для системы здравоохранения, связанное с затратами на лечение. Охват населения вакцинацией против ветряной оспы (ВО) и опоясывающего герпеса (ОГ) остается низким по ряду причин, включая отсутствие достаточного количества вакцин. Совершенствование качества существующих и создание новых генно-инженерных, эффективных препаратов с высоким профилем безопасности, а также усовершенствование протоколов их оценки с включением в алгоритмы параметров клеточного иммунного ответа являются необходимым условием развития вакцинопрофилактики заболеваний, вызываемых ВВО. Систематизация данных о текущем статусе вакцин против ВО и ОГ поможет разработчикам в планировании дизайна доклинических и клинических исследований.
ЦЕЛЬ. Анализ опыта разработки и внедрения в клиническую практику современных вакцин для профилактики заболеваний, вызываемых вирусом ветряной оспы, а также оценка путей дальнейших разработок профилактических вакцин.
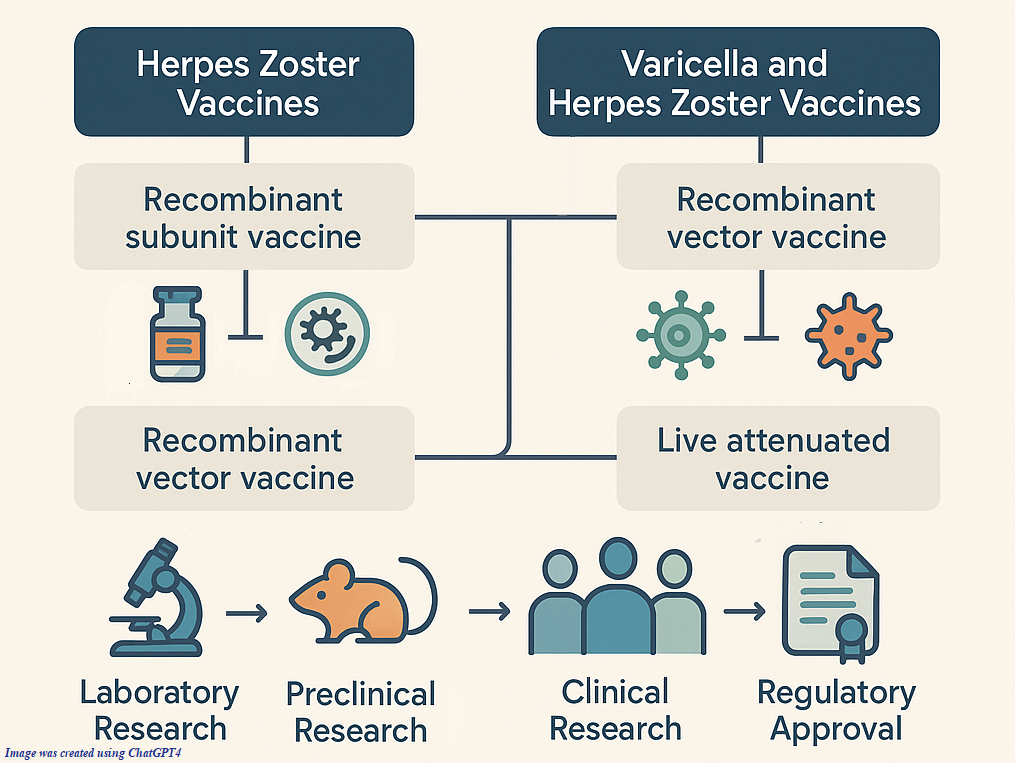
ОБСУЖДЕНИЕ. Для профилактики ВО и ОГ рекомендуют применять живые вакцины, поскольку они имитируют естественный иммунный ответ организма на контакт с вирусным агентом и активируют как гуморальный, так и клеточный иммунитет. В настоящее время в мире зарегистрировано семь живых вакцин для профилактики ВО и две живые вакцины для профилактики ОГ. Однако при сниженном иммунитете ввиду различных состояний живые вакцины не рекомендованы из-за возможного развития вакциноассоциированных заболеваний. Рекомбинантная вакцина на основе вирусного гликопротеина Е c системой адъювантов показана для профилактики ОГ для лиц старше 50 лет с возможностью назначения иммунокомпрометированным пациентам.
ЗАКЛЮЧЕНИЕ. Наиболее перспективными являются исследования в области разработок вакцин на основе рекомбинантных, РНК-, ДНК-технологий. Поскольку безопасность данных вакцин по ряду параметров превосходит живые вакцины, применение их возможно у лиц с ослабленным иммунитетом. В России также ведется работа по созданию вакцин против ВВО-ассоциированных заболеваний.
ISSN 2619-1156 (Online)